
目前,生物可降解生物材料被广泛用于骨再生。然而,如何根据骨愈合阶段准确调整其降解率以实现骨再生仍是一项重大挑战。本项研究介绍了一种新型生物可降解骨移植物,该移植物与沸石咪唑框架-8(ZIF-8)纳米晶体结合在一起,通过微注射成型制造,微型注塑促使PLGA中的PCL原位成纤以提供增强效果,同时纳米级ZIF-8还能控制PLGA的降解。分子动力学模拟和实验结果均表明,ZIF-8纳米晶体中的Zn2+可作为路易斯酸参与PLGA基质的降解,从而成功调和了基质降解与增强相保持之间的矛盾。此外,纳米ZIF-8改良骨移植物还能改善血管生成-骨生成耦合。在体外,它能直接促进内皮细胞(ECs)的HIF-1α和毛细血管样网络的形成,以及骨髓间充质干细胞(BMSCs)中RUNX2和OCN的表达。在体内,含有中等浓度(0.5%)ZIF-8纳米粒子的骨移植物通过与骨愈合阶段相匹配的可调生物降解来帮助血管化骨再生。
课题组李怡俊副教授和四川大学华西口腔陈俊宇教授领导的研究团队,运用微型注塑挤出成型工艺成功制备了具有原位微纤结构的PLGA/PCL@nZ材料。如图1所示,在制备过程中,PCL在PLGA基体中原位成纤,这一简便而有效的方法能够在材料中形成微纤结构,赋予材料力学性能增强特性。分子动力学模拟显示ZIF-8能够起到路易斯酸的作用,催化PLGA降解,同时由于PCL的微纤化作用,平衡了降解与力学性能关系,对后续适配骨愈合过程提供了基础。
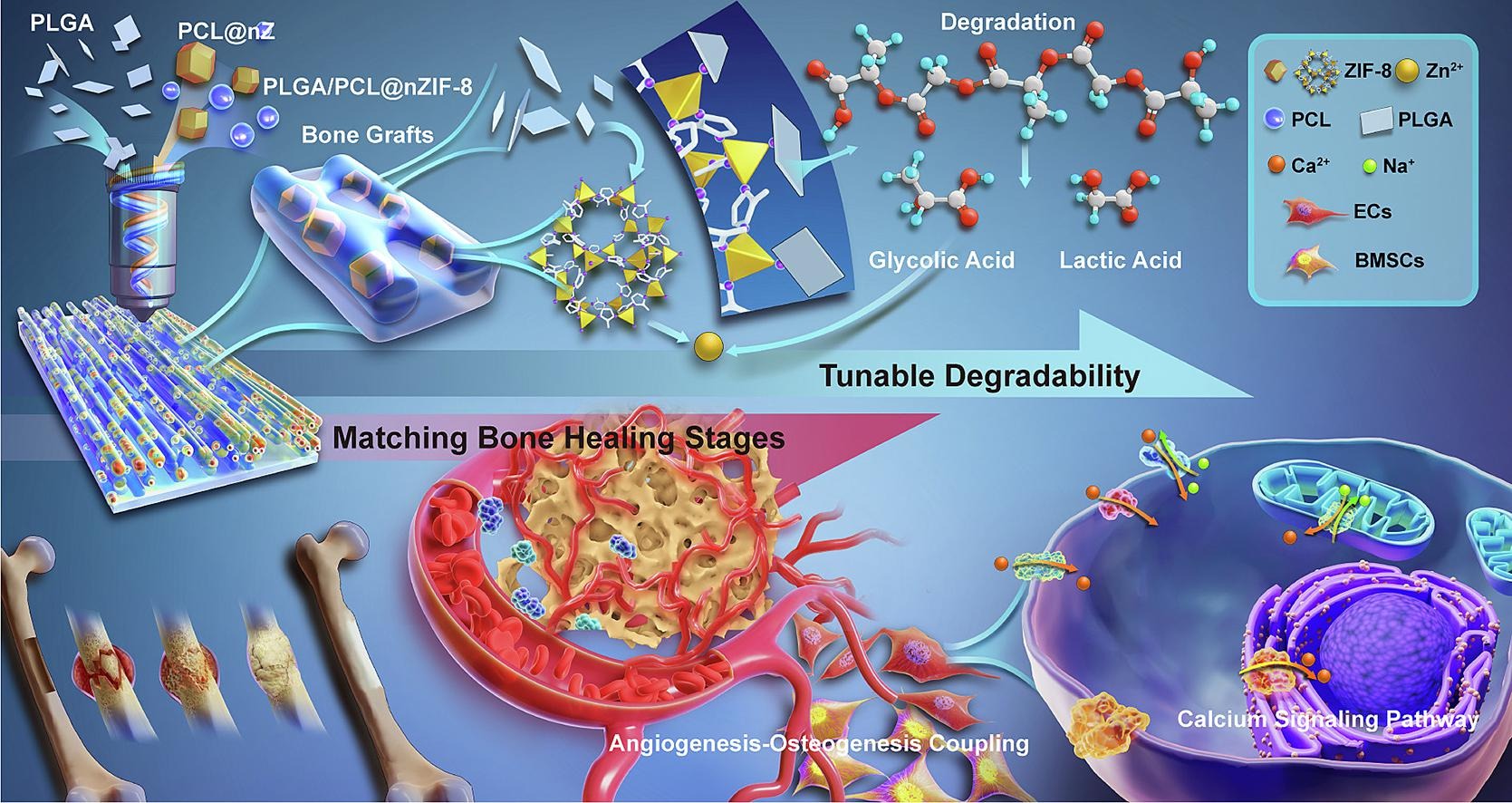
图1 PLGA/PCL@nZ制备及骨愈合应用示意图
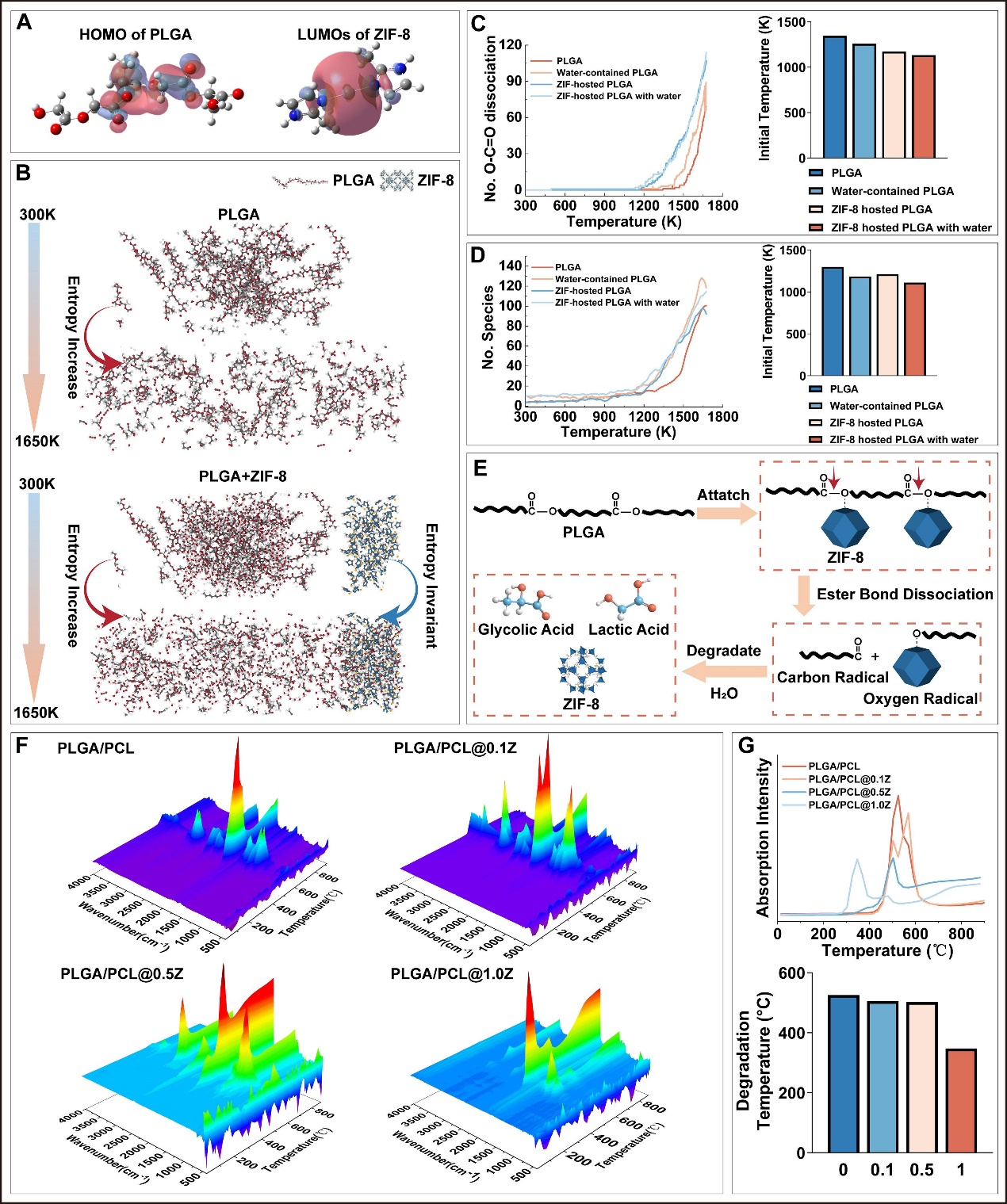
图2 评估微注射成型 PLGA/PCL@nZ 骨移植物的降解机制
研究表明,纳米级ZIF-8改性微注射成型骨移植物在骨缺损修复方面具有显著优势。首先,适当浓度的纳米级ZIF-8(0.5 %)可通过上调ALP、促进钙盐沉积、增加RUNX2和OCN表达来增强成骨细胞分化,从而帮助骨愈合。其次,调节纳米级ZIF-8的含量可以调整PLGA/PCL@nZ骨移植材料的降解率,使其与骨愈合进程相一致。骨缺损中材料的降解率会影响骨愈合的结果。材料的快速降解(PLGA/PCL@1.0Z)会损害其机械支撑力,增加骨段脱位。相反,降解缓慢则表明材料(PLGA/PCL)占据空间,阻碍骨细胞迁移,限制新骨生长,破坏机械负荷分布,可能导致应力屏蔽,影响骨愈合。确定了0.5%是ZIF-8纳米晶体的最佳浓度,能产生最有效的骨愈合效果。
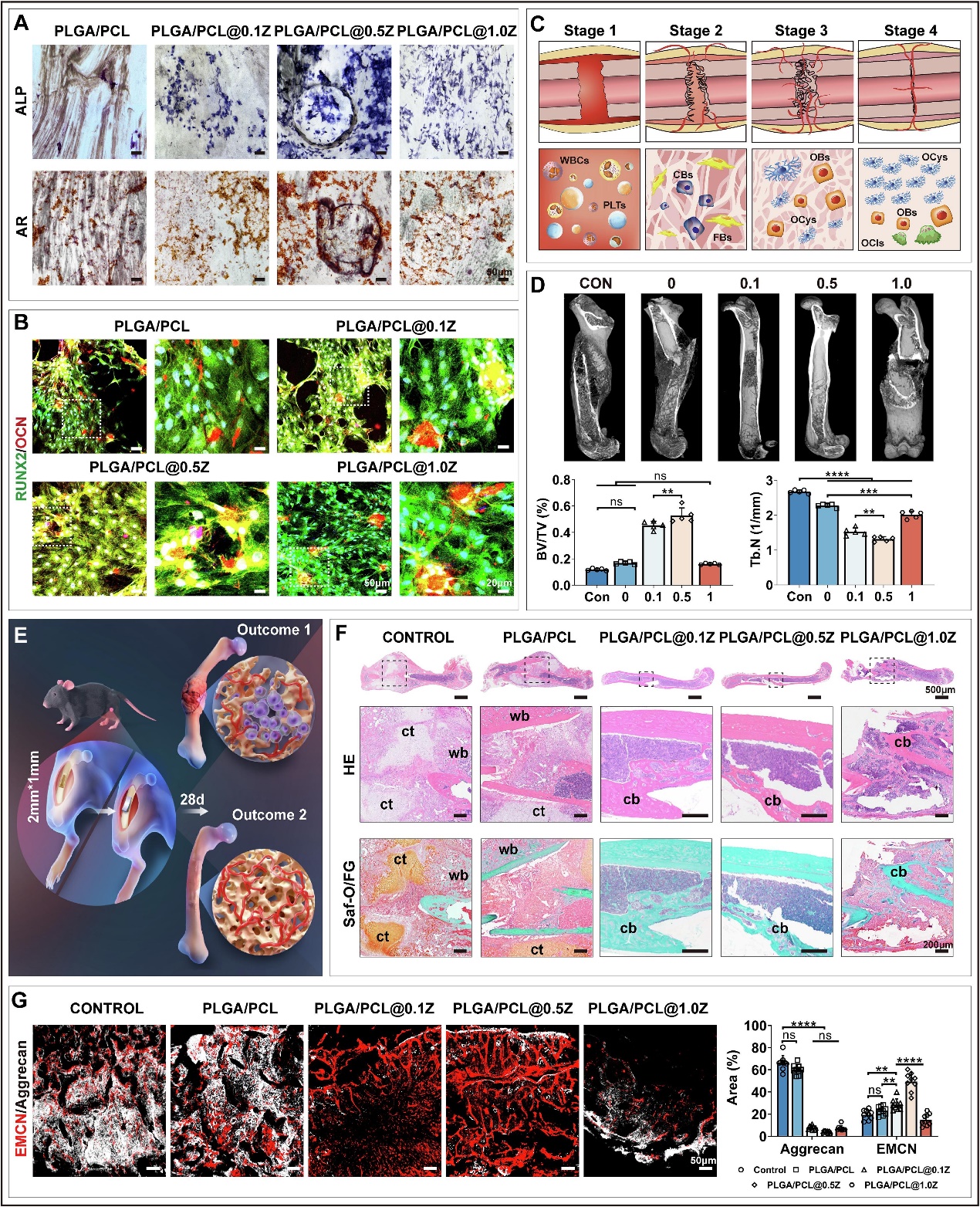
图3 微型注射成型PLGA/PCL@nZ骨移植物促成骨细胞潜力的体外和体内评估
PLGA/PCL复合材料采用微注塑工艺制备,PCL在PLGA基体中原位成纤,同时ZIF-8纳米晶体在其中能起到调控降解作用,最终制成了新型的 PLGA/PCL@nZ骨移植物。ZIF-8纳米晶体中的Zn2+被鉴定为路易斯酸,与 LUMO一致,而 PLGA 的HOMO则以其酯结构为中心。ZIF-8纳米粒子中的 Zn2+作为路易斯酸参与了PLGA基质的降解。在体外,接枝物促进了血管生成过程EC中HIF-1α的表达,并增强了成骨过程BMSCs中RUNX2和OCN的表达。在体内,PLGA/PCL@nZ骨移植物通过共同调节ECs和BMSCs中的钙信号通路并使材料降解与愈合同步,促进了骨愈合。综上所述,本研究提出了一种新型、可调控、可降解的生物活性骨移植物,具有重要的临床意义。
该研究成果以“Biomimetic management of bone healing stages: MOFs induce tunable degradability and enhanced angiogenesis-osteogenesis coupling”为题发表在学术期刊Chemical Engineering Journal上,四川大学博士生盖阔以及硕士生张桐瑞为共同第一作者,课题组李怡俊副教授和四川大学华西口腔陈俊宇教授、蔡和助理研究员为共同通讯作者。